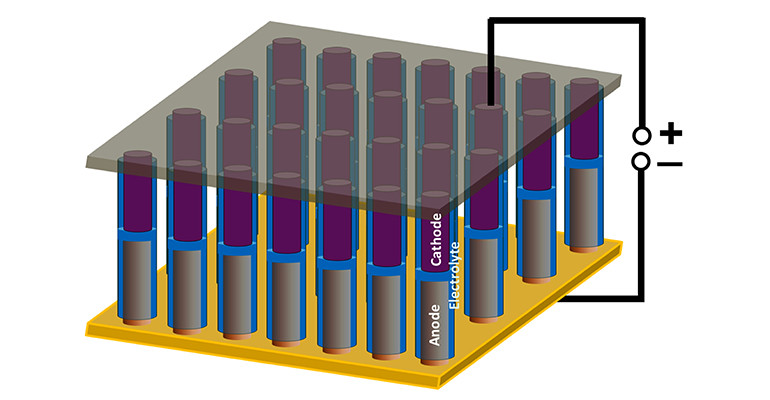
Czego dokładnie potrzeba (patrz rysunek powyżej)? Otóż podłoża miedzianego z dołkami (będzie to jedna strona baterii). Następnie niklu bądź cyny do uformowania anod baterii w kształcie walca opartych o te dołki (kolor szary). W dalszej kolejności tlenku polietylenu w formie żelu, aby wytworzyć cienką warstwę separującą anody, stanowiącą elektrolit baterii (kolor niebieski). I jeszcze polianiliny do ukształtowania jej katod, także w formie walca, ponad wspomnianym tlenkiem (kolor fioletowy). Wreszcie tylko folii aluminiowej do położenia na katody (druga strona baterii) i gotowe! Prawda, że proste? No pewnie, dopóki nie zda się sprawy ze skali, w której trzeba całość zrealizować. Ta wynosi setki nanometrów i mniej, więc „metody domowe” odpadają. W grę wchodzi tylko laboratorium naukowe z dobrej klasy mikroskopem elektronowym przewidzianym do tego rodzaju zadań. Lecz nawet jeśli, to liczba cykli ładowań i rozładowań baterii jest niska - wynosi ona jedynie 20. Czy to się opłaca?
Cóż, zawsze jest coś za coś – w tym przypadku jest to miniaturyzacja kosztem sprawności. Na szczęście ostatnie można zwiększyć eksperymentując z materiałami i ich grubościami. Jest to cel przyświecający obecnie naukowcom na świecie. Ci zresztą odkryli ponad dwukrotne wydłużanie się anod z dwutlenku cyny podczas ładowania baterii. Zaobserwowano to szczególnie w 2010 roku w amerykańskim instytucie badawczym Sandia National Laboratories, który udostępnił nawet zdjęcie pokazujące wspomniane zjawisko. Zdjęcie to jest dostępne poniżej. Warto na nie spojrzeć. Jaka szkoda, że w budowie opisanej baterii nie może pomóc ś.p Adam Słodowy, który z pewnością byłby dumny z niniejszego tekstu utrzymanego w duchu jego pokazów telewizyjnych. Kto wie czy nawet nie ulepszyłby on wynalazku - przynajmniej byłoby widać, że majsterkowanie jest w istocie dla każdego. Takie to zasilanie!